|
Asma
EPIGENÉTICA E ASMA
A asma é um sério problema de saúde global devido à alta morbidade e ao controle inadequado da doença que acomete todas as faixas etárias. Sua prevalência está aumentando em muitos países, especialmente entre crianças. Embora alguns países tenham observado um declínio nas hospitalizações e mortes por asma, esta doença ainda impõe um ônus inaceitável aos sistemas de saúde e à sociedade pela perda de produtividade no local de trabalho, pelos dias de escola perdidos e pelos problemas que acarretam às famílias.
Dados do estudo epidemiológico internacional ISAAC corroboram essas diferenças geográficas na prevalência da asma, sugerindo que o ambiente e a epigenética desempenham papel relevante em pacientes com essa doença.1

O termo epigenética foi
proposto pela primeira vez
pelo biólogo inglês
Conrad H. Waddington (Figura 1) em 1942
que estava interessado em entender como os genes interagiam com seu ambiente para produzir características fenotípicas.2
Definição e Conceitos Fundamentais
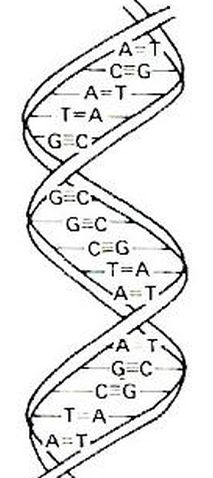
A definição contemporânea de epigenética abrange o estudo de alterações hereditárias na função gênica que não envolvem modificações na sequência do DNA (Figura 2). Ela examina a origem das modificações na estrutura da cromatina. Em outras palavras, a epigenética investiga como fatores externos e internos podem influenciar a atividade dos genes, afetando o fenótipo de um organismo.3 Para usar uma metáfora, a genética refere-se à escrita dos genes, a epigenética à sua leitura. A genética refere-se à sequência do DNA, a "escrita" da informação genética, enquanto a epigenética modula a "leitura" dessa informação, determinando quais genes são expressos e em que momento.
 Os mecanismos epigenéticos são responsáveis pela 'identidade' de nossas células, mas também podem ajudar a determinar quem somos. Por exemplo, gêmeos homozigotos, que compartilham o mesmo material genético, exatamente o mesmo DNA, são, no entanto, desiguais, devido aos fatores epigenéticos que causam pequenas diferenças próprias para cada indivíduo. Os mecanismos epigenéticos são responsáveis pela 'identidade' de nossas células, mas também podem ajudar a determinar quem somos. Por exemplo, gêmeos homozigotos, que compartilham o mesmo material genético, exatamente o mesmo DNA, são, no entanto, desiguais, devido aos fatores epigenéticos que causam pequenas diferenças próprias para cada indivíduo.
Embora os fenômenos epigenéticos sejam parte da nossa vida cotidiana e essenciais para a manutenção da saúde, suas alterações podem contribuir para o desenvolvimento de doenças como câncer, doenças metabólicas, psiquiátricas, doenças autoimunes e inflamatórias, incluindo a asma.
A epigenética, um campo de estudo em rápida expansão, explora a intrincada interação entre o comportamento (dieta, tabagismo, estresse etc.), o ambiente em sentido amplo e a função gênica.
Através de um processo totalmente diferente das mutações genéticas, que alteram a sequência do DNA, as mudanças epigenéticas podem ser transmitidas durante as divisões celulares, sendo dinâmicas, reversíveis, modulando a expressão gênica sem alterar a estrutura do genoma e são potencialmente transmissíveis de uma geração a outra.4
Estas modificações se processam através de mecanismos reguladores da transcrição, com metilação do DNA, modificação de histonas e modificação pós-transcricional usando microRNA (miRNA) ou pequeno RNA interferente (siRNA) em primeiro plano.
Os Mecanismos Epigenéticos Mais Estudados Incluem
■ Metilação do DNA: É um dos principais mecanismos epigenéticos. Adição de "grupos metil" (CH3: um átomo de carbono e três átomos de hidrogênio) em nucleotídeos que formam a sequência de DNA, o que pode mudar a atividade de um segmento de DNA, sem mudar a sequência. Quando situada em um promotor de gene, a metilação do DNA normalmente age para reprimir a transcrição do gene.3
■ Modificações de histonas:
As histonas, principais proteínas da cromatina, organizam o DNA em estruturas compactas. Modificações químicas nessas proteínas regulam a acessibilidade dos genes, determinando sua ativação ou repressão. Mecanismos epigenéticos controlam a compactação da cromatina e atuam nas regiões reguladoras do DNA, modulando a expressão gênica sem alterar a sequência genética.
■ Regulação da transcrição genética por microRNAs:
Os microRNAs, diferentemente do RNA mensageiro ou ribossômico, são RNAs muito curtos (em média 22 nucleotídeos) que possuem uma sequência complementar ao RNA mensageiro. Eles podem regular a tradução do RNA mensageiro ou, alternativamente, levar à sua degradação.5,6
Genética na Asma
Com o avanço da tecnologia de sequenciamento genômico, pesquisadores intensificaram seus esforços para compreender e prever a complexidade e heterogeneidade da asma, tornando os estudos de associação do genoma completo (GWAS) a abordagem preferida. Esses estudos tiveram um impacto significativo na epigenética ao identificar variantes associadas à asma e revelar como essas variações interagem com mecanismos epigenéticos.
O primeiro GWAS sobre asma foi publicado em 2007 por Moffatt et al.,7 identificando uma associação entre variações genéticas no cromossomo 17q12-21 e a asma infantil. Esses polimorfismos foram relacionados à expressão do gene ORMDL3 e, posteriormente, ligados a outros genes, como GSDMA, GSDMB, CRKRS, ZBPB2 e IKZF2.37-39 Esse lócus mostrou-se especificamente associado à asma de início na infância, mas não à de início tardio.8,9
Em 2010, o estudo GABRIEL,10 um dos maiores GWAS sobre asma, analisou mais de 26 mil indivíduos e identificou genes em diversos cromossomos relacionados à doença, incluindo IL1RL1/IL18R1 (cromossomo 2), HLA-DQ (cromossomo 6), IL33 (cromossomo 9), SMAD3 (cromossomo 15), ORMDL3/GSDMB (cromossomo 17) e IL2RB (cromossomo 22). O ORMDL3 foi fortemente associado à asma infantil, enquanto o HLA-DQ foi correlacionado à asma de início tardio. O estudo concluiu
que as variantes no lócus ORMDL3/GSDMB estão vinculadas exclusivamente à asma de início infantil, enquanto a elevação dos níveis séricos totais de IgE exerce um papel secundário no desenvolvimento da doença.10
Em uma metanálise de um GWAS incluindo norte-americanos de ascendência europeia, afro-americana ou afro-caribenha e latina identificaram cinco loci de suscetibilidade. Quatro previamente relatados (17q21, perto de IL1RL1, TSLP e IL33) associados ao risco de asma em três grupos étnicos. Identificaram, entretanto, um novo lócus de suscetibilidade à asma em PYHIN1, com a associação sendo específica para indivíduos de ascendência africana.11
Uma revisão em 2020 compilou dados de GWASs e identificou 128
polimorfismos de nucleotídeo único (SNPs) associados à asma,12 ampliando o conhecimento sobre a base genética da doença. É notável que a maioria dos GWASs sobre asma tenha sido conduzida em populações de ascendência europeia, enquanto estudos envolvendo outros grupos étnicos permanecem limitados. Há necessidade de novas pesquisas focadas em populações de ascendência não europeia.
Os estudos GWASs desempenham função importante na epigenética, pois ajudam a identificar regiões genômicas associadas a doenças e características complexas, permitindo investigar mecanismos epigenéticos envolvidos na regulação da expressão gênica. Ao integrar dados de metilação, expressão gênica e fatores ambientais, esses estudos ajudam a desvendar como mutações e o ambiente interagem para influenciar doenças complexas, como a asma.
Aqui estão algumas maneiras pelas quais os GWASs contribuem para a epigenética:
1. Identificação de Regiões Reguladoras e Variantes Funcionais
• A maioria das variantes genéticas identificadas pelos GWASs se encontra em regiões reguladoras do DNA, como promotores, enhancers e regiões de ligação de fatores de transcrição, em vez de regiões codificantes.
• Muitas dessas variantes influenciam a epigenética, regulando a metilação do DNA, as modificações de histonas e a atividade de microRNAs (miRNAs).
Exemplo: No lócus 17q21, associado à asma, variantes identificadas por GWASs estão em regiões que regulam a expressão de ORMDL3 e GSDMB, que modulam a inflamação por mecanismos epigenéticos.13
2. Mapeamento de Regiões Diferencialmente Metiladas (DMPs)
• Os GWASs podem ser combinados com estudos epigenômicos, como EWASs (Epigenome-Wide Association Studies), que analisam diferenças na metilação do DNA associadas às doenças.
• GWAS identifica SNPs associados à asma, mas a maioria das variantes está em regiões não codificantes, o que dificulta a determinação de sua função.
• EWAS analisa padrões de metilação do DNA em pacientes com e sem asma para encontrar locais epigeneticamente modificados que podem influenciar a expressão gênica.
A integração dos dois tipos de estudos ajuda a responder:
• O SNP regula diretamente a expressão do gene?
⇒ Se um SNP identificado no GWAS for um eQTL (expression QTL), ele pode afetar a expressão gênica sem envolver a epigenética.
• O SNP influencia a metilação do DNA?
⇒ Se for um mQTL (methylation QTL), ele pode modular padrões epigenéticos, afetando indiretamente a expressão gênica e o risco de asma.
• A metilação altera a expressão sem SNPs envolvidos?
⇒ Isso sugere que a epigenética atua independentemente da variação genética.
Concluindo:
✓ |
Se um SNP afeta diretamente a expressão gênica ⇒ GWAS + eQTLs (efeito genético direto) |
✓ |
Se um SNP altera a metilação do DNA, que por sua vez regula a expressão gênica ⇒ GWAS + mQTLs + EWAS (efeito epigenético mediado por genética) |
✓ |
Se a metilação do DNA ocorre independentemente de SNPs ⇒ EWAS sugere influência ambiental (efeito epigenético puro) |
Isso fortalece a ideia de que a asma tem uma base multifatorial, combinando genética e influências ambientais via epigenética.
Exemplo: No estudo que conduziu uma EWAS abrangente para identificar locais de metilação do DNA associados à asma em adultos, os autores analisaram amostras de sangue de 2.286 participantes, categorizando-os em grupos com asma atópica, não atópica, atopia sem asma e um grupo de referência sem atopia ou asma. Os resultados revelaram numerosos sítios CpG diferencialmente metilados associados tanto à asma atópica quanto à não atópica, implicando novos genes e vias relacionadas ao sistema nervoso e à inflamação.14
• Isso ajuda a distinguir se um SNP afeta diretamente a doença ou se age por meio de mecanismos epigenéticos.
3. Integração com Dados de Expressão Gênicas (eQTLs)
• Os GWASs são frequentemente combinados com perfis de expressão gênica (eQTLs loci de características quantitativas de expressão) para compreender como as variantes genéticas influenciam a atividade dos genes-alvo.
• Isso ajuda a revelar se a regulação é mediada por mecanismos epigenéticos, como:
• Metilação do DNA
• Modificações de histonas
• Interação entre RNA não codificantes e DNA
Exemplo:
Em 2023, pesquisadores realizaram uma análise de eQTLs utilizando dados transcriptômicos e genotípicos de 433 pacientes coreanos com asma. Ao integrar esses dados com resultados de GWAS, foram identificados 15 genes específicos relacionados à asma na população coreana estudada. Este trabalho destaca a importância de considerar contextos populacionais e estados de doença ao investigar interações genético-epigenéticas na asma.15
4. Descoberta de Interação Gene-Ambiente
• A epigenética atua na interface entre o genoma e o ambiente, e os GWASs podem identificar regiões do DNA onde exposições ambientais (poluentes, tabagismo, dieta) modulam a metilação do DNA ou a acessibilidade à cromatina.
• Isso permite entender como fatores externos podem modificar o risco genético de doenças.
Exemplos: Estudo cruzado duplo-cego investigou o impacto da exposição de curto prazo ao ao escapamento de diesel na metilação do DNA de
células mononucleares do sangue periférico em 16 indivíduos asmáticos, não fumantes. Demonstraram alteração na metilação de 2.827 locais CpG, após a exposição, mas não ao ar filtrado. Resultou em alta metilação do DNA afetando genes GSTP1, elementos repetitivos Alu e LINE1, relacionados à inflamação e ao estresse oxidativo, reforçando a relevância da epigenética para entender os efeitos das exposições ambientais na expressão genética.16,17
Epigenética, Ambiente e Asma
O crescente número de publicações nesta área evidencia o interesse científico em aprofundar a compreensão da relação entre o sistema imunológico e os efeitos ambientais através de fenômenos epigenéticos. De fato, o estudo dos fenômenos epigenéticos parece explicar parte das variações fenotípicas observadas na mesma doença.
Nos últimos 15 anos, a genética da asma passou por uma transformação significativa impulsionada por estudos genômicos. Em 2022, uma análise abrangente de 22 biobancos revelou 179 loci, incluindo 49 novos, associados a fenótipos de asma, oferecendo valiosa compreensão sobre a complexa base genética da doença.18
Citamos alguns estudos em humanos de mecanismos epigenéticos na asma, com foco especial na metilação do DNA:
Estudos epigenéticos sobre asma infantil identificaram assinaturas de metilação específicas associadas à inflamação alérgica nas vias aéreas e células imunológicas, evidenciando o papel regulador da metilação na patogênese da asma. Apesar dessas descobertas, pesquisas adicionais sobre os mecanismos epigenéticos subjacentes aos endótipos da asma, ainda são necessárias.
Para esses estudos, principalmente em crianças, as  células epiteliais do nariz são mais fáceis de acessar do que as dos brônquios, permitindo a coleta de amostras com técnicas menos invasivas.19 Por isso, grande parte das informações sobre a metilação do DNA nas vias aéreas na asma infantil vem de estudos com o epitélio nasal.20 Forno et al. identificaram um painel de 30 CpGs em uma coorte de 483 crianças em idade escolar em Porto Rico, capaz de prever atopia e asma atópica,21 com aplicabilidade clínica futura na previsão de asma no bebê chiador. células epiteliais do nariz são mais fáceis de acessar do que as dos brônquios, permitindo a coleta de amostras com técnicas menos invasivas.19 Por isso, grande parte das informações sobre a metilação do DNA nas vias aéreas na asma infantil vem de estudos com o epitélio nasal.20 Forno et al. identificaram um painel de 30 CpGs em uma coorte de 483 crianças em idade escolar em Porto Rico, capaz de prever atopia e asma atópica,21 com aplicabilidade clínica futura na previsão de asma no bebê chiador.
Alterações nos microRNAs estão associadas à hiper-responsividade brônquica em asmáticos. Estudos através de lavado brônquico revelam diferenças substanciais nos perfis de miRNA exossômico entre indivíduos saudáveis e pacientes com asma estável e leve. Esses miRNA regulam vias de sinalização inflamatória (via MAPK e JAK/STAT) e a expressão de citocinas (IL-6, IL-8, IL-10, IL-13), que desempenham um papel direto na patogênese da asma.21 Esses resultados indicam relação entre o ambiente e a desregulação inflamatória em pacientes asmáticos.22 O perfil de expressão dos miRNAs alterados foi altamente correlacionado com a função pulmonar (VEF1) nesses indivíduos (R = 0,74). Por outro lado no mesmo estudo a exposição ao ar do metrô,
uma fonte conhecida de importante emissão de matéria particulada, não causou nenhuma alteração significativa nos perfis de miRNA.22
Indivíduos que carregam certas variantes genéticas na região 17q12-q21 apresentam um risco aumentado de desenvolver asma de início precoce, e o número dessas variantes deletérias que um indivíduo possui está diretamente relacionado à idade em que a asma se manifesta pela primeira vez na infância. No entanto, a expressão clínica da asma pode variar consideravelmente entre os indivíduos, mesmo que compartilhem marcadores genéticos semelhantes na mesma região. Fatores como exposição precoce à fumaça ambiental do tabaco e infecções virais na infância, desempenham atribuições relevantes na modulação da expressão da asma.23 Curiosamente, a interação gene-ambiente a gatos na primeira infância demonstrou atenuar o risco de asma de início precoce em indivíduos geneticamente predispostos a desenvolver a doença.24
A expressão dos alelos da asma também pode ser influenciada pela origem parental, com estudos demonstrando associação entre asma e rinite em casos de transmissão paterna.25 Essa descoberta destaca a importância de examinar a história familiar e os padrões de herança ao investigar a genética da asma.
Um número crescente de elementos sustenta uma causalidade entre exposição a transtorno pós-traumático em nível individual ou comunitário e estresse psicossocial associados à maior morbidade da asma. Foi o que evidenciou estudo nos EUA em que fatores de estresse psicossocial crônicos, frequentemente presentes na vida de indivíduos em vulnerabilidade econômica e minorias étnicas, contribuem de forma desproporcional para maior incidência da asma nesse grupo. Constatou-se que a exposição à violência estava associada à metilação dentro de um promotor (ADCYAP1R1), que estava correlacionado à presença de asma nesta mesma população.26 Existem evidências sugerindo a existência de genes de suscetibilidade que predispõem jovens cronicamente estressados ao transtorno de estresse pós-traumático e à asma.27 Décadas de pesquisa demonstram que os estressores percebidos como ameaçadores e incontroláveis alteram a atividade do eixo hipotálamo-hipófise-adrenal (HPA) e do sistema nervoso autônomo (SNA).26
Em resumo, a revolução na genética da asma proporcionou uma compreensão mais profunda da complexa interação entre fatores genéticos e ambientais que moldam o desenvolvimento e a progressão da doença. Esses avanços não apenas esclarecem os mecanismos subjacentes à asma, mas também abrem caminho para abordagens mais personalizadas e eficazes no diagnóstico, tratamento e prevenção da asma.
Embora a epigenética tenha fornecido insights valiosos sobre a asma, não há nenhum tratamento aprovado específico epigenético para asma como acontece para o câncer onde miRNAs supressores de tumor são silenciados, permitindo a ativação de oncogenes, ou na hipertensão no controle do sistema renina-angiotensina.
Referências
01.Mallol J, Crane J, von Mutius E, Odhiambo J, Keil U, Stewart A; ISAAC Phase Three Study Group. The International Study of Asthma and Allergies in Childhood (ISAAC) Phase Three: a global synthesis. Allergol Immunopathol (Madr) 2013; 41:73-85.
02.Waddington CH. The epigenotype. 1942. Int J Epidemiol 2012; 41:10-3.
03.Yang IV, Lozupone CA, Schwartz DA. The environment, epigenome, and asthma. J Allergy Clin Immunol 2017; 140:14-23.
04.Épigénétique - Inserm, La Science pour la Santé - Épigénétique. Un génome, plein de possibilité! Disponível em:https://www.inserm.fr/dossier/epigenetique/
05.Martino D, Kesper DA, Amarasekera M, et al. Epigenetics in immune development and in allergic and autoimmune diseases. J Reprod Immunol 2014; 104105:438.
06.Ambros V. microRNAs: tiny regulators with great potential. Cell 2001; 107:8236
07.Moffatt MF, Kabesch M, Liang L, Dixon AL, Strachan D, Heath S, Depner M, von Berg A, Bufe A, Rietschel E, Heinzmann A, Simma B, Frischer T, Willis-Owen SA, Wong KC, Illig T, Vogelberg C, Weiland SK, von Mutius E, Abecasis GR, Farrall M, Gut IG, Lathrop GM, Cookson WO. Genetic variants regulating ORMDL3 expression contribute to the risk of childhood asthma. Nature 2007; 448:47073.
08.Ferreira MAR, Mathur R, Vonk JM, et al. Genetic architectures of childhood- and adult-onset asthma are partly distinct. Am J Hum Genet 2019; 104:66584.
09.Pividori M, Schoettler N, Nicolae DL, Ober C, Im HK. Shared and distinct genetic risk factors for childhood-onset and adult-onset asthma: genome-wide and transcriptome-wide studies. Lancet Respir Med 2019; 7:50922.
10.Moffatt MF, Gut IG, Demenais F, Strachan DP, Bouzigon E, Heath S, von Mutius E, Farrall M, Lathrop M, Cookson WOCM; GABRIEL Consortium. A large-scale, consortium-based genomewide association study of asthma. N Engl J Med 2010; 363:1211-1221.
11.Torgerson DG, Ampleford EJ, Chiu GY, Gauderman WJ, Gignoux CR, Graves PE et al. Meta-analysis of genome-wide association studies of asthma in ethnically diverse North American populations. Nat Genet 2011; 43:887-92.
12.El-Husseini ZW, Gosens R, Dekker F, Koppelman GH. The genetics of asthma and the promise of genomics-guided drug target discovery. Lancet Respir Med 2020; 8:P1045-1056.
13.Bouzigon E, Corda E, Aschard H, Dizier MH, Boland A, Bousquet J, Chateigner N, Gormand F, Just J, Le Moual N, Scheinmann P, Siroux V, Vervloet D, Zelenika D, Pin I, Kauffmann F, Lathrop M, Demenais F. Effect of 17q21 variants and smoking exposure in early-onset asthma. N Engl J Med 2008; 359:1985-94.
14.Hoang TT, Sikdar S, Xu CJ, Lee MK, Cardwell J, Forno E, Imboden M, Jeong A, Madore AM, Qi C, Wang T, Bennett BD, Ward JM, Parks CG, Beane-Freeman LE, King D, Motsinger-Reif A, Umbach DM, Wyss AB, Schwartz DA, Celedón JC, Laprise C, Ober C, Probst-Hensch N, Yang IV, Koppelman GH, Londres SJ. Estudo de associação de todo o epigenoma de metilação do DNA e asma adulta no Agricultural Lung Health Study. Eur Respir J 2020; 56(3):2000217.
15.Kim DJ, Lim JE, Jung HU, Chung JY, Baek EJ, Jung H, Kwon SY, Kim HK, Kang JO, Park K, Won S, Kim TB, Oh B. Identification of asthma-related genes using asthmatic blood eQTLs of Korean patients. BMC Med Genomics 2023; 16:259.
16.Jiang R, Jones MJ, Sava F, Kobor MS, Carlsten C. Short-term diesel exhaust inhalation in a controlled human crossover study is associated with changes in DNA methylation of circulating mononuclear cells in asthmatics. Part Fibre Toxicol 2014; 11:71.
17.Valinluck V, Tsai H-H, Rogstad DK, Burdzy A, Bird A, Sowers LC: Oxidative damage to methyl-CpG sequences inhibits the binding of the methyl-CpG binding domain (MBD) of methyl-CpG binding protein 2 (MeCP2). Nucleic Acids Res 2004, 32:41004108.
18.Tsuo K, Zhou W, Wang Y, Kanai M, Namba S, Gupta R, Majara L, Nkambule LL, Morisaki T, Okada Y, Neale BM; Global Biobank Meta-analysis Initiative; Daly MJ, Martin AR. Multi-ancestry meta-analysis of asthma identifies novel associations and highlights the value of increased power and diversity. Cell Genom 2022; 2:100212.
19.Hudon Thibeault AA, Laprise C. Cell-Specific DNA Methylation Signatures in Asthma. Genes (Basel). 2019; 10:932.
20.Ntontsi P, Photiades A, Zervas E, Xanthou G, Samitas K. Genetics and Epigenetics in Asthma. Int J Mol Sci 2021; 22:2412.
21.Forno E, Wang T, Qi C, Yan Q, Xu CJ, Boutaoui N, Han YY, Weeks DE, Jiang Y, Rosser F, Vonk JM, Brouwer S, Acosta-Perez E, Colón-Semidey A, Alvarez M, Canino G, Koppelman GH, Chen W, Celedón JC. DNA methylation in nasal epithelium, atopy, and atopic asthma in children: a genome-wide study. Lancet Respir Med 2019; 7:336-346.
22.Levänen B, Bhakta NR, Torregrosa Paredes P, Barbeau R, Hiltbrunner S, Pollack JL, Sköld CM, Svartengren M, Grunewald J, Gabrielsson S, Eklund A, Larsson BM, Woodruff PG, Erle DJ, Wheelock ÅM. Altered microRNA profiles in bronchoalveolar lavage fluid exosomes in asthmatic patients. J Allergy Clin Immunol 2013; 131:894-903.
23.Bouzigon E, Corda E, Aschard H, Dizier MH, Boland A, Bousquet J, Chateigner N, Gormand F, Just J, Le Moual N, Scheinmann P, Siroux V, Vervloet D, Zelenika D, Pin I, Kauffmann F, Lathrop M, Demenais F. Effect of 17q21 variants and smoking exposure in early-onset asthma. N Engl J Med 2008; 359:1985-94.
24.Stokholm J, Chawes BL, Vissing N, Bønnelykke K, Bisgaard H. Cat exposure in early life decreases asthma risk from the 17q21 high-risk variant. J Allergy Clin Immunol 2018; 141:1598-1606.
25.Sarnowski C, Sugier PE, Granell R, Jarvis D, Dizier MH, Ege M, Imboden M, Laprise C, Khusnutdinova EK, Freidin MB, Cookson WOC, Moffatt M, Lathrop M, Siroux V, Ogorodova LM, Karunas AS, James A, Probst-Hensch NM, von Mutius E, Pin I, Kogevinas M, Henderson AJ, Demenais F, Bouzigon E. Identification of a new locus at 16q12 associated with time to asthma onset. J Allergy Clin Immunol 2016; 138:1071-1080.
26.Chen W, Boutaoui N, Brehm JM, Han YY, Schmitz C, Cressley A, Acosta-Pérez E, Alvarez M, Colón-Semidey A, Baccarelli AA, Weeks DE, Kolls JK, Canino G, Celedón JC. ADCYAP1R1 and asthma in Puerto Rican children. Am J Respir Crit Care Med 2013; 187:584-8.
27.Rosenberg SL, Miller GE, Brehm JM, Celedón JC. Stress and asthma: novel insights on genetic, epigenetic, and immunologic mechanisms. J Allergy Clin Immunol 2014; 134:1009-15.
|