|
Asma
Tratamento da Asma
DOSES E EFEITOS COLATERAIS DOS CORTICOIDES
A partir da década de 1980 o uso de corticoides inalatórios (CI) tornou-se universalmente aceito como a melhor terapêutica primária de manutenção para pacientes com asma persistente, pois são liberados diretamente no local onde ocorre a inflamação a mucosa brônquica. São drogas que controlam efetivamente a inflamação das vias aéreas, melhoram os parâmetros das provas de função pulmonar, reduzem os sintomas, as exacerbações e a necessidade de medicamentos de resgate.
O controle da asma por um CI requer a liberação homogênea da droga tanto nas grandes como pequenas vias aéreas, pois as mesmas anormalidades celulares e histopatológicas, assim como a hiper-responsividade brônquica, estão presentes em toda a árvore respiratória. A dose deve ser individualizada para cada paciente. Na Tabela 1 são apresentadas as faixas de doses diárias de CI utilizadas para adultos, adolescente e crianças entre 6 e 11 anos, de acordo com a gravidade da doença (ver manejo da asma) e a equipotência para os diferentes corticoides comercializados na atualidade. Deve ser ressaltado que o tabaco reduz os efeitos dos CI em fumantes ativos e em ex-fumantes, devendo suas doses serem ajustadas. Estes pacientes devem ser alertados que o fumo reduz a ação da terapêutica.
Tabela 1 – Doses dos Corticoides Inalatórios para Adultos e Adolescentes
|
Adultos e Adolescentes ( a partir de 12 anos ) |
Dose diária total de CI (mcg) |
DROGA |
Baixa |
Média |
Alta |
| Dipropionato Beclometasona (spray, partícula padrão, HFA) |
200–500 |
>500–1000 |
>1000 |
| Dipropionato Beclometasona (IP, spray, partícula extrafina, HFA) |
100–200 |
>200–400 |
>400 |
| Budesonida (IP, spray, partícula padrão, HFA) |
200–400 |
>400–800 |
>800 |
| Ciclesonida (spray, partícula extrafina, HFA) |
80–160 |
>160–320 |
>320 |
| Furoato Fluticasona (IP) |
100 |
200 |
| Propionato Fluticasona (IP) |
100–250 |
>250–500 |
>500 |
| Propionato Fluticasona (spray, partícula padrão, HFA) |
100–250 |
>250–500 |
>500 |
| Mometasona Furoato (IP) |
200 |
400 |
| Mometasona Furoato (spray, partícula padrão, HFA) |
200–400 |
>400 |
Crianças 6–11 anos de idade
|
| Dipropionato Beclometasona (spray, partícula padrão, HFA) |
100–200 |
>200–400 |
>400 |
| Dipropionato Beclometasona (spray, partícula extrafina, HFA) |
50–100 |
>100–200 |
>200 |
| Budesonida (IP) |
100–200 |
>200–400 |
>400 |
| Budesonida (nebulizador) |
250–500 |
>500–1000 |
>1000 |
| Ciclesonida (spray, partícula extrafina, HFA) |
80 |
>80–160 |
>160 |
| Furoato Fluticasona (IP) |
50 |
n.a |
| Propionato Fluticasona (IP) |
50–100 |
>100–200 |
>200 |
| Propionato Fluticasona (spray, partícula padrão, HFA) |
50–100 |
>100–200 |
>200 |
| Mometasona Furoato (spray, partícula padrão, HFA) |
100 |
200 |
Esta NÃO
pressupõe uma equivalência de potência.
P. ex., a transição de uma dose "média" de um corticoide inalatório para uma dose "média" de outro não garante uma potência equivalente. Tal mudança pode resultar em diminuição (ou aumento) da eficácia, levando a uma possível instabilidade da asma do paciente (ou aumento do risco de efeitos adversos).
|
| CI: corticoide inalatório; HFA: propelente hidrofluoroalcano; IP: inalante de pó; n.a.: não aplicável. |
O tratamento com CI em doses baixas é geralmente mais benéfico para a maioria das crianças com asma, oferecendo uma série de vantagens. No entanto, o aumento das doses desses medicamentos está correlacionado com maior risco de efeitos adversos, tanto locais como sistêmicos. Portanto, é importante encontrar um equilíbrio adequado entre os potenciais benefícios terapêuticos e os possíveis efeitos colaterais ao considerar opções de tratamento.
Tabela 2 – Doses Diárias Baixas de Corticoides Inalatórios para Crianças de 5 Anos ou Menos
|
Faixa etária com dados adequados de segurança e eficácia |
DROGA |
Dose diária total de CI (mcg) |
Dipropionato Beclometasona (spray, partícula padrão, HFA) |
100 (5 anos ou mais)
|
Dipropionato Beclometasona (spray, partícula extrafina, HFA) |
50 (5 anos ou mais)
|
Budesonida (nebulizador) |
500 (maiores de 1 ano)
|
Propionato Fluticasona (spray, partícula padrão, HFA) |
50 (4 anos ou mais)
|
Mometasona Furoato (spray, partícula padrão, HFA) |
100 (5 anos ou mais)
|
Ciclesonida (spray, partícula extrafina, HFA) |
Não suficientemente avaliado em crianças de 5 anos ou menos
|
Em crianças o spray deve sempre ser utilizado com um espaçador
Os dados sobre potência comparativa não estão ainda disponíveis, especialmente para crianças e esta tabela NÃO implica, portanto, equivalência de potência.
|
Estudos químicos e físicos sobre aerossóis demonstram a importância do tamanho das partículas inaladas. Segundo Taburet e Schmit,1 partículas maiores que 10 µm depositam-se na boca e orofaringe, enquanto que partículas menores que 0,5 µm alcançam os alvéolos, sendo exaladas sem se depositar na superfície brônquica. Partículas de 1 a 5 µm são as ideais, depositando-se nas pequenas vias aéreas cumprindo o seu papel terapêutico. Para os pacientes com obstrução brônquica, como ocorre na asma, as partículas não devem ultrapassar 2 a 3 µm. A deposição dos aerossóis faz-se através da difusão Browniana.
Para o tratamento da asma os CI estão disponíveis em três formulações: pó seco, em suspensão líquida e em solução. Os medicamentos em pó seco podem ser divididos em inaladores de dose única e inaladores de dose múltipla, diferenciando-se apenas na facilidade de uso e quantidade de doses entre eles. Nos inaladores de dose única, o medicamento vem embalado em cápsulas, associados a excipientes como a lactose. Os corticoides por inalação em suspensão e solução estão disponíveis em sprays dosimetrados, livrando partículas padrão ou extrafina.
Quando da aplicação do jato do spray, somente uma pequena parcela do medicamento se deposita nos pulmões. O restante é deglutido e absorvido pelo tubo gastrintestinal e inativado pela passagem através do fígado. Alguns CI como a budesonida e a fluticasona, apresentam metabolização muito eficiente durante esta primeira passagem, com inativação de 89% e 99%, respectivamente. Todavia, alguns corticoides não são convenientemente inativados por este processo, resultando em alta biodisponibilidade sistêmica com efeitos extrapulmonares inconvenientes.
Objetivando-se evitar a impactação na orofaringe, reduzindo-se o número de partículas maiores de 10 µm que chegam até a boca, utilizam-se sprays acoplados a espaçadores de grande volume (média 750 ml) ou dispositivos para inalação da droga sob a forma de pó seco. Aperfeiçoamentos recentes na tecnologia dos sprays resultaram em formulação na qual a droga é dissolvida em uma solução. Dispositivos em solução liberam maior proporção de partículas respiráveis (isto é, partículas menores do que 5 µm de diâmetro) do que os tradicionais dispositivos em suspensão.
Quando da utilização de sprays com o propelente clorofluorocarbono (CFC) aproximadamente 10–30% da dose administrada alcançam os pulmões, enquanto que o restante se deposita na orofaringe e é deglutido. Alguns sprays veiculados com o propelente hidrofluoralcano (HFA) exibem maior deposição, podendo alcançar 50%,2 alcançando com melhor eficiência as pequenas vias aéreas. O uso de sprays que utilizam o propelente HFA acoplados ao espaçador dobra a deposição do corticoide nas vias aéreas.3 Esta melhor performance pode levar a um menor custo de tratamento, se for necessária menor quantidade da droga, para manter o controle da asma.
Os espaçadores (Figura 1) são câmaras de inalação utilizadas para minimizar a má utilização dos sprays. São reservatórios de plástico ou metal que acumulam em suspensão o medicamento nebulizado. Sua eficiência está relacionada ao tamanho, ao volume, à baixa carga eletrostática, à forma e a sua correta utilização. O espaçador permite que o aerossol seja inalado através de uma válvula bucal, durante inspiração única ou como recomendado  para crianças, durante o volume corrente. Durante a expiração a válvula fecha-se. A inalação através do espaçador deve ser feita imediatamente, pois a meia-vida da droga liberada pelo spray na câmara do espaçador é menor que 10 segundos. Outro aspecto técnico para o uso do espaçador de grande volume é a abolição do efeito de inércia do aerossol. O espaçador aumentando a distância entre a spray e as vias aéreas aumenta a distância a ser percorrida pelo aerossol, lentificando-o e permitindo que o propelente se evapore. Isto reduz o tamanho das partículas, enquanto que as maiores (não-respiráveis) que se impactariam na faringe ficam retidas no espaçador. Espaçadores de pequeno volume reduzem também a velocidade das partículas inaladas porém, são menos eficazes em aumentar a fração que chega aos pulmões. para crianças, durante o volume corrente. Durante a expiração a válvula fecha-se. A inalação através do espaçador deve ser feita imediatamente, pois a meia-vida da droga liberada pelo spray na câmara do espaçador é menor que 10 segundos. Outro aspecto técnico para o uso do espaçador de grande volume é a abolição do efeito de inércia do aerossol. O espaçador aumentando a distância entre a spray e as vias aéreas aumenta a distância a ser percorrida pelo aerossol, lentificando-o e permitindo que o propelente se evapore. Isto reduz o tamanho das partículas, enquanto que as maiores (não-respiráveis) que se impactariam na faringe ficam retidas no espaçador. Espaçadores de pequeno volume reduzem também a velocidade das partículas inaladas porém, são menos eficazes em aumentar a fração que chega aos pulmões.
Os espaçadores desenvolvem uma carga eletrostática que reduz consideravelmente a quantidade de droga disponível para o paciente. Os modelos mais recentes são fabricados com material que não apresenta carga eletrostática. Para reduzir este problema com os espaçadores de plástico e para aumentar a sua eficiência, eles devem ser lavados com detergentes, sendo a sua secagem somente por escoamento do líquido da lavagem, sem utilizar toalhas de tecido ou papel.
Os inaladores de pó são comumente usados para a administração de medicamentos inalados e devem fornecer doses consistentes e eficientes, serem fáceis de usar corretamente e serem apreciados pelos pacientes; todos esses atributos podem afetar a adesão do paciente e, portanto, a eficácia do tratamento.
As suas principais vantagens são a maior facilidade de uso, a sua portabilidade e compacidade. O pó é mais estável do que as soluções porém, a formulação de partículas secas mais finas é mais difícil devido a sua instabilidade física e tendência a coesão e adesão, o que pode diminuir a performance do aerossol. Os dispositivos de inalação de pó seco dependem do esforço inspiratório do paciente, sendo que de 15 a 32% da dose administrada alcançam os pulmões.4 O fluxo inspiratório requerido para uma eficiente utilização depende do dispositivo utilizado. Em geral os dispositivos de pó seco são de mais fácil utilização, pelos pacientes (principalmente idosos e crianças), do que os sprays, pois não requerem coordenação entre a liberação da medicação e a inspiração. Um fluxo inspiratório de 30 l min-1 é necessário para o uso eficiente do Ellipta e Turbhaler. Outros dispositivos como o Accuhaler/Diskus e Clickhaler necessitam de um fluxo menor, cerca de 20 l min-1. Deve ser ressaltado, entretanto, que todos os dispositivos de pó seco são fluxo-dependentes, atuando melhor com fluxos inspiratórios de 60 l min-1. Pacientes com obstrução grave não conseguem alcançar fluxos máximos, comprometendo a deposição do medicamento, da mesma forma que crianças menores de cinco anos têm dificuldade em obter fluxo inspiratório mínimo de 30 l min-1.
Para os pacientes incapazes de utilizar os dispositivos de pó que demandam baixo fluxo inspiratório, resta a nebulização com aparelho equipado com bocal ou máscara adequados. Para a utilização de corticoide por nebulização, dispomos no comércio da budesonida e da beclometasona em suspensão para aerossolterapia. O nebulizador deve ser conectado a um compressor de ar com fluxo adequado (6–8 l/min), assegurando partículas de 2 a 5 μm e volume de câmara de 2-4 ml. Os nebulizadores ultrassônicos não são adequados para a administração de suspensão de corticoide. A dose diária total de budesonida para adultos é de 1–2 mg (2–4 ml da suspensão a 0,50 mg/ml). Deve-se adicionar soro fisiológico a 0,9% para completar o volume da câmara de 2 a 4 ml. A dose de beclometasona é de 1 flaconete – 2 ml (0,4 mg/ml) – a cada administração, 1 ou 2 vezes ao dia. O paciente deve enxaguar a boca após a administração. Caso seja utilizada máscara facial, o paciente deve certificar-se de que a máscara se encaixa perfeitamente enquanto estiver sendo feita a inalação, devendo lavar o rosto após o seu término.
Os achados de inflamação também em pequenas vias aéreas distais (< 2mm de diâmetro) proporcionam questionamentos quanto à ação dos corticoides por inalação na periferia do pulmão, o que ainda não foi bem estabelecido. Esmailpour et al.5 investigaram a deposição do propionato de fluticasona nos tecidos pulmonares centrais e periféricos obtidos em asmáticos submetidos à cirurgia torácica. Este estudo revelou maior concentração da droga em tecidos centrais. Uma potencial solução para uma melhor e mais homogênea distribuição pode ser obtida pela alteração do propelente utilizado para veicular o corticoide, alterando-se o tamanho da partícula livrada. Leach et al.2 demonstraram que a beclometasona veiculada pelo hidrofluoroalcane (HFA) alcançava a periferia de uma forma mais eficaz do que quando veiculada em clorofluorcarbono (CFC), elevando significativamente a biodisponibilidade pulmonar da droga. Existem poucos estudos que abordam a maior deposição de pequenas partículas de corticoides nas pequenas vias aéreas. Deve ser destacada a rica vascularização dos bronquíolos terminais e alvéolos, capaz de aumentar a quantidade de droga absorvida que passa para a circulação, elevando a biodisponibilidade sistêmica e em consequência os efeitos adversos dos corticoides.
Os mecanismos pelos quais os corticoides inalados exercem seus efeitos farmacológicos são os mesmos para todas as drogas atualmente encontradas no mercado. Entretanto, o que pode influenciar o resultado final são as propriedades farmacocinéticas, que variam nas substâncias disponíveis. As características farmacocinéticas englobam a biodisponibilidade, o clearance, a meia-vida e a capacidade de ligação proteica no plasma. Ainda não dispomos da droga ideal, cujas propriedades, entretanto, são conhecidas. Esta droga teria as seguintes características farmacocinéticas e farmacodinâmicas: baixa biodisponibilidade oral, baixa biodisponibilidade sistêmica, alta biodisponibilidade pulmonar, alta afinidade com os receptores de corticoides, alta ligação proteica plasmática, estrutura de pró-droga, grande volume de distribuição, alta conjugação lipídica, alta afinidade lipídica, rápido clearance sistêmico, alta potência intrínseca, alta deposição pulmonar, longo tempo de permanência em tecido broncopulmonar e pequenas partículas.
Efeitos Colaterais dos Corticoides por Inalação
Recomenda-se titular a dose do CI e manter a mais baixa e efetiva capaz de manter o controle da asma de cada paciente. |
|
a) Locais
Os efeitos colaterais podem ser divididos em locais e sistêmicos. Os locais são decorrentes da ação do corticoide na pele (dermatite perioral) e na mucosa da orofaringe. O mais comum é a candidíase oral e esofagiana, determinando sintomas em 5% dos pacientes.6 A sintomatologia na faringe manifesta-se por irritação e pela dor, às vezes agravada pela deglutição (odinofagia) e pela disfagia. Sua ocorrência pode ser reduzida com o uso do espaçador e utilização do medicamento antes das principais refeições, ou lavando-se a boca imediatamente após a inalação. Os efeitos colaterais locais são proporcionais à quantidade do corticoide inalado e ao número de doses diárias. Esquemas terapêuticos com duas tomadas diárias causam muito menos candidíase do que aqueles com quatro doses por dia.
Outro efeito local é a disfonia6 decorrente de miopatia dos músculos da laringe, sendo dose dependente. Os problemas da voz são minimizados quando da utilização de dispositivos para inalação que utilizam o corticoide em pó,7 sendo mais acentuados com os sprays, já que ao contrário da candidíase, o espaçador não protege contra a disfonia. Esta constatação parece ser devido ao dispositivo utilizado. Os inaladores de pó seco fazem com que o paciente inale contra uma resistência, alterando a posição anatômica das estruturas acima da laringe, modificando também a posição das cordas vocais, mantendo-as abertas, o que pode influenciar na deposição das partículas da droga. Com o spray, com ou sem espaçador, isso não acontece.
A tosse que é uma manifestação clínica frequente na asma também pode ocorrer quando da utilização de corticoide tópico, não diretamente relacionada à droga inalada, porém ao efeito tóxico de excipientes, como o ácido oleico, utilizado como surfactante. A tosse durante a inspiração é mais comum com o spray com ou sem espaçador de grande volume. Os inaladores de pó seco raramente determinam tosse quando livram partículas finas, entretanto, a tosse pode estar presente quando do uso de dispositivos de pó seco que contenham grandes quantidades de lactose.
Os efeitos locais dependem da substância utilizada. O dipropionato de beclometasona e a ciclesonide determinam menos efeitos locais por serem inaladas como droga inativa, como pró-drogas, sendo convertidas à forma ativa somente nos pulmões.
A hipertrofia da língua é uma complicação raramente descrita. Tem sido relatada principalmente em crianças tratadas com a budesonida.8 Acredita-se que ocorra por ação direta do corticoide sobre o músculo da língua, determinando sua hipertrofia e acúmulo local de gordura, sendo facilmente reversível após a suspensão do medicamento.
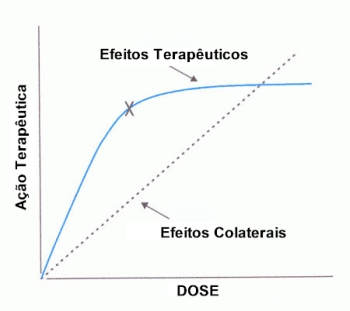 Existem duas limitações no que concerne ao uso dos corticoides por inalação que merecem ser salientadas. Primeira – embora pequenas doses de corticoide por inalação sejam bastante efetivas, o benefício de altas doses é limitado. Dobrando-se ou quadruplicando-se a dose do corticoide, pode ocorrer melhora substancial no quadro clínico e consequente controle da doença porém, com aumento considerável dos efeitos colaterais. Segunda – a utilização de altas doses por longo tempo pode causar efeitos sistêmicos adversos, como a osteoporose que predispõe às fraturas, à catarata, ao glaucoma, à pneumonia, às alterações cardiovasculares, além de interferir no crescimento das crianças e na síntese dos hormônios sexuais. Existem duas limitações no que concerne ao uso dos corticoides por inalação que merecem ser salientadas. Primeira – embora pequenas doses de corticoide por inalação sejam bastante efetivas, o benefício de altas doses é limitado. Dobrando-se ou quadruplicando-se a dose do corticoide, pode ocorrer melhora substancial no quadro clínico e consequente controle da doença porém, com aumento considerável dos efeitos colaterais. Segunda – a utilização de altas doses por longo tempo pode causar efeitos sistêmicos adversos, como a osteoporose que predispõe às fraturas, à catarata, ao glaucoma, à pneumonia, às alterações cardiovasculares, além de interferir no crescimento das crianças e na síntese dos hormônios sexuais.
Na Figura 2 demonstra-se a relação entre os efeitos benéficos e o surgimento dos efeitos colaterais à medida que se aumenta a dose do corticoide por inalação.
b) Sistêmicos
Quanto aos efeitos colaterais sistêmicos os mais relatados são a interferência no eixo hipófise-suprarrenal, intolerância à glicose, osteoporose, adelgaçamento da pele, estrias, acne, catarata, ganho de peso, hipertensão arterial, edemas e em crianças o retardo no crescimento. Sob condições normais, a secreção média diária de cortisol pelas adrenais em adultos é a equivalente a 5 mg de prednisona. Desta forma, doses de corticoides > 5 mg/dia são consideradas suprafisiológicas e podem aumentar os riscos de efeitos adversos.
Com doses de beclometasona ou budesonida não superiores a 800 mcg/dia, praticamente não há alteração significativa nos níveis de cortisol plasmático matinal, ou excreção urinária em 24 horas de cortisol livre.9-11 Vários estudos com doses mais elevadas foram efetuados, destacando-se o de Brown et al.12 que avaliaram um grupo de nove voluntários normais e concluíram que para uma dose de 2.000 mcg/dia de beclometasona ocorre redução significante na excreção urinária do cortisol em 24 h, fato este que não ocorreu com o uso de budesonida. Johanson et al. 13 estudaram a supressão do cortisol matinal pela beclometasona e budesonida em 12 voluntários normais, com inalação de doses 400 mcg, 800 mcg e 3.200 mcg/dia. A supressão ocorreu unicamente com doses acima das terapêuticas. A comparação de 2.000 mcg/dia de fluticasona com 2.000 mcg/dia de beclometasona evidenciou que ambas causam pequena supressão no eixo hipófise-suprarrenal, mantendo-se, entretanto, os níveis médios de cortisol dentro da faixa normal.
Recentemente a aplicação de perfis metabolômicos em larga escala, utilizando dados de quatro coortes de 14.000 indivíduos com asma, analisou os efeitos do tratamento dos CIs nos níveis dos metabólitos esteroides de acordo com a dose.14 Os efeitos do tratamento com CIs nos níveis destes metabólitos foram dependentes da dose; entretanto demonstraram significativas reduções também com o tratamento com a baixa dose de CI.14 A supressão adrenal pode ser diagnosticada por manifestar fadiga, anemia e hiperpigmentação cutânea. Recomenda-se o monitoramento regular do cortisol matinal.
O uso prolongado de corticoide pode levar à osteoporose em pacientes de qualquer idade, reduzindo o volume ósseo com desestruturação da arquitetura trabecular tridimensional, afetando principalmente os ossos do quadril, punho, costelas e as vértebras torácicas e lombares. A estabilidade óssea depende de um perfeito equilíbrio entre a formação do osso pelos osteoblastos e sua reabsorção por osteoclastos. Estes processos são regulados por vários mediadores, incluindo hormônios, citocinas e outros agentes. Os corticoides apresentam uma ação bifásica sobre o osso. Inicialmente estimulam a reabsorção e após longo tempo de tratamento, suprimem a sua formação.
O corticoide reduz a absorção de cálcio pelos intestinos e a reabsorção pelos rins, determinando maior excreção urinária do cálcio, ocorrendo, como consequência, o aumento da secreção do hormônio da paratireoide, que atua nos osteoclastos determinando absorção óssea. O uso de corticoide por via oral suprime os osteoblastos e afeta a síntese adrenal de estrogênio. Os CIs não apresentam efeitos tão intensos na absorção do cálcio intestinal ou nos níveis do paratormônio. Todavia, apresentam efeito supressivo significativo nos androgênios adrenais, incluindo androstenediona e dehidroepiandrosterona (DHEA), essenciais na formação óssea da mulher na pós-menopausa.
Cerca de 30 a 50% dos pacientes que fazem uso crônico de corticoides desenvolvem osteoporose. Os CIs, quando utilizados em doses acima das terapêuticas e por longo período, podem também causar osteoporose, sendo o grupo de mulheres na menopausa o mais atingido. Quando da associação de corticoide tópico e oral, o risco aumenta.15 A osteoporose induzida por corticoides pode ser monitorizada através da densitometria óssea. Adequada suplementação de cálcio e vitamina D deve ser mantida. Para as mulheres em menopausa, preconiza-se 1.000 a 1.500 mg de cálcio e 400 U de vitamina D por dia. Na Tabela 3 são apresentadas as recomendações para o manejo da osteoporose.
Como a perda óssea associada aos corticoides ocorre predominantemente nos primeiros seis meses de tratamento, recomenda-se a avaliação densitométrica no início e já aos seis meses, utilizando-se medidas profiláticas desde o início de sua utilização.
Os corticoides induzem à apoptose de osteócitos. Outra complicação relativamente comum decorrente da sua utilização é a osteonecrose, também conhecida como necrose avascular ou necrose asséptica. A cabeça do fêmur é o sítio mais acometido por este processo, podendo ocorrer também na cabeça do úmero e no fêmur distal. Este processo ocorre por acúmulo de osteócitos apoptóticos, que resulta em colapso da cabeça do fêmur.
Tabela 3 Recomendações para o Tratamento da Osteoporose
Recomendações para o Tratamento da Osteoporose |
▰ Dar preferência ao corticoide por inalação. Se houver necessidade do corticoide oral empregar sempre a menor dose |
| ▰ Exposição solar |
| ▰ Completar a dieta com suplementação diária de cálcio até 1.500 mg em duas tomadas por dia |
| ▰ A associação de cálcio e vitamina D é eficiente na diminuição da incidência de fraturas |
| ▰ Incentivar o exercício. Isométricos os recomendados para evitar debilidade proximal |
| ▰ Reposição hormonal, sob supervisão, na menopausa e naquelas com baixa dosagem de estradiol (pré-menopausa). Nos homens avaliar os níveis de testosterona |
| ▰ Prescrever um diurético tiazídico para controlar a hipercalciúria |
| ▰ Efetuar densitometria óssea antes de iniciar o tratamento e anualmente, para assegurar a sua eficácia |
| ▰ Se ocorrer perda óssea apesar do tratamento apropriado, ou não for possível a reposição hormonal, considerar outro tratamento utilizando os bifosfonatos |
| ▰ Na falha ou intolerância aos bifosfonatos, o denosumabe está indicado no tratamento de mulheres com osteoporose na pós-menopausa |
É reconhecido que os CIs são um fator de risco independente para a pneumonia na DPOC.16,17 Entretanto para a asma, o risco foi descrito somente quando foram utilizadas doses elevadas de CI.18
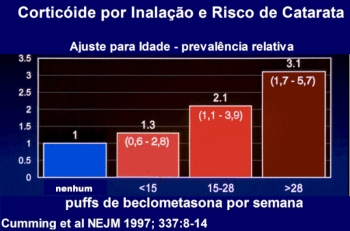 A catarata subcapsular posterior é outra complicação conhecida após uso prolongado de corticoides por via sistêmica. No momento estão em curso estudos que avaliam se o uso dos corticoides por via inalatória pode também determiná-la. Cumming et al.19 concluíram que o uso de corticoide, mesmo por inalação, está associado ao desenvolvimento de catarata subcapsular e nuclear (Figura 2). O glaucoma pode também ser induzido ou exacerbado pela administração de corticoides. A catarata subcapsular posterior é outra complicação conhecida após uso prolongado de corticoides por via sistêmica. No momento estão em curso estudos que avaliam se o uso dos corticoides por via inalatória pode também determiná-la. Cumming et al.19 concluíram que o uso de corticoide, mesmo por inalação, está associado ao desenvolvimento de catarata subcapsular e nuclear (Figura 2). O glaucoma pode também ser induzido ou exacerbado pela administração de corticoides.
O crescimento e a função adrenal em crianças é pouco afetado quando do uso em doses preconizadas, 400 mcg de beclometasona, 600 mcg de budesonida e 200 mcg de fluticasona. Deve ser salientada, no entanto, a possibilidade de uma importante variação individual na resposta sistêmica ao CI.
Wolthers et al.20 apresentaram estudo em que compararam o efeito da fluticasona e beclometasona sobre o crescimento dos membros inferiores, obtendo resultado significativamente maior para o propionato de fluticasona. Acredita-se que a asma severa e malcontrolada é capaz por si só de retardar o crescimento da criança,21 enquanto que crianças sob tratamento tópico desenvolvem-se normalmente. Mesmo que os corticoides inalados interfiram no crescimento de algumas crianças, a sua instituição precoce pode prevenir a necessidade futura de corticoide por via oral, quando as doses são mais potentes e mais tóxicas. Recomenda-se o acompanhamento seriado por endocrinologista para toda a criança que necessite de CI, em dose diária ≥ 400 µg de beclometasona, ou dose equivalente de outro corticoide.
É sabido que o uso prolongado de corticoides por via sistêmica está associado a um grande risco de diabetes em pacientes predispostos. A intolerância à glicose está relacionada a um aumento da produção de glicose hepática (gliconeogênese), redução na utilização da glicose periférica e aumento da resistência da insulina, com inibição dos efeitos da insulina nos miócitos e adipócitos. Os efeitos dos corticoides inalados no metabolismo da glicose ainda não estão bem determinados, embora pareçam ser doses dependentes.
Os efeitos cardiovasculares têm sido associados ao uso prolongado de doses moderadas a altas de CIs em regime diário. Esse impacto está relacionado à forma como os receptores de corticosteroides são ativados no organismo. A ativação excessiva desses receptores pode contribuir para o desenvolvimento de resistência à insulina, hipertensão e dislipidemia.22 Assim como ocorre na Síndrome de Cushing,22-24 há relatos de um risco elevado de embolia pulmonar, incluindo pacientes em tratamento com corticoides, como no caso de tratamento para asma.
Baixas doses sistêmicas e altas doses de corticoides inalados podem determinar púrpura e também um adelgaçamento da pele,25 que se torna facilmente vulnerável a pequenas contusões. Seis semanas de terapia com corticoides inalados são suficientes para conter a síntese de colágeno da pele.26 Haapasaar et al.27 avaliaram os efeitos na síntese de colágeno e espessura da pele de pacientes com asma após 1 a 2 anos de moderadas doses de corticoides inalados, tendo confirmado a redução na síntese, porém não detectaram mudanças significantes na espessura e quantidade total do colágeno da pele.
Existem vários relatos de distúrbios psiquiátricos concomitantes ao uso por inalação dos corticoides. Dentre eles incluem-se: labilidade emocional, euforia, depressão, agressividade e insônia.
É importante que as recomendações das diretrizes para usar a menor dose efetiva de CIs sejam observadas. Na eventualidade de doses moderadas-altas, na asma severa, para pacientes malcontrolados, apesar de boa adesão ao tratamento, a eficácia e a segurança associadas aos biológicos fazem com que sua utilização seja uma opção a ser considerada.28
Referências
01.Taburet AM, Schmit B. Pharmacikinetic optimization of asthma treatment. Clin Pharmacokinet 1994; 26:396-418.
02.Leach CL, Davidson PJ, Bourdreau RJ. Improved airway targeting with the CFC-free HFA-beclomethasone metered-dose inhaler compared with CFC-beclomethasone. Eur Respir J 1998; 12:1346-53.
03.Toogood JH, White FA, Baskerville JC, Fraher LJ, Jennings B. Comparison of the anti-asthmatic, oropharyngeal, and systemic glucocorticoid effects of budesonide administered through a pressurized aerosol plus spaer or the Turbuhaler dry powder inhaler. J Allergy Clin Immunol 1997;99:186-93.
04.Barnes PJ, Pedersen S, Busse WW. Efficacy and safety of inhaled corticosteroids. New developments. Am J Respir Crit Care Med 1998; 157:S1-S53.
05.Esmailpour N, Hogger P, Rabe KF, Heitmenn U, Nakashima M, Rohdewald P. Distribution of inhaled fluiticasone propionate between human lung tissue and serum in vivo . Eur Respir Dis J 1997; 10:1496-9.
06.Williams AJ, Baghat MS, Stableforth DE, Cayton RM, Shenoi PM, Skinner C. Dysphonia caused by inhaled steroids: recognition of a characteristic laryngeal abnormality. Thorax 1983; 38:813-21
07.Selroos O, Backman R, Forsén KO, Löfroos AB, Niemistö M, Pietinalho A, Aikäs C, Riska H. Local side-effects during 4-year treatment with inhaled corticosteroids-a comparison between pressurized metered-dose inhalers and Turbuhaler. Allergy 1994; 49:888-90.
08.Dubus JC, Marguet C, Deschildre A, Mely L, Le Roux P, Brouard J, Huiart L. Local side effects of inhaled corticosteroids in asthmatic children: influence of drug, dose, age and device. Allergy 2001; 56:944-8.
09.Geddes DM. Inhaled corticosteroids: benefits and risks. Thorax 1992; 47:404-7.
10.Lofdahl CG, Mellstrand T, Svedmyr N. Glucocorticoids and asthma. Studies of resistance and systemic effects of glucocorticoids. Eur J Respir Dis 1984; 65:69-79.
11.Warner J, Nikolaizik W, Marchant J. The systemic effects of inhaled corticosteroids. J Allergy Clin Immunol 1989; 83:220-25.
12.Brown PH, Matusiewicz SP, Shearing C, Tibi L, Greening AP, Crompton G. , Systemic effects of high dose inhaled steroids: Comparison of beclomethasone dipropionate and budesonide in healthy subjects. Thorax 1993; 48:967-73.
13.Johansson SA., Andersson KE, Brattsand R, Gruvstads E, Hedner P. Topical and systemic glucocorticoid potencies of budesonide and beclomethasone dipropionate in man. Eur J Clin PharmacoL 1982; 22:523-9.
14.Kachroo P, Stewart ID, Kelly RS, et al. Metabolomic profiling reveals extensive adrenal suppression due to inhaled corticosteroid therapy in asthma. Nat Med 2022 28, 814822.
15.Hosking DJ. Effects of corticosteroids on bone turnover. Respir Dis 1993; 87(suppl A):15-20.
16.Christenson SA, Smith BM, Bafadhel M, Putcha N. Chronic obstructive pulmonary disease. Lancet 2022; 399:2227-2242.
17.Ritchie AI, Singayagam A, Mitchell S, Wedzicha JA, Shah A, Bloom CI. The Effect of Inhaled Corticosteroids on Pneumonia Risk in Patients With COPD-Bronchiectasis Overlap: A UK Population-Based Case-Control Study. Chest 2023; 164:875-884.
18.O'Byrne PM, Pedersen S, Carlsson LG, Radner F, Thorén A, Peterson S, Ernst P, Suissa S. Risks of pneumonia in patients with asthma taking inhaled corticosteroids. Am J Respir Crit Care Med 2011; 183:589-95.
19.Cumming RG, Mitchell P, Leeder SR. Use of inhaled corticosteroids and the risk of cataracts. NEJM 1997; 337:8-14.
20.Wolthers OD, Pedersen S. Short term growth during treatment with inhaled fluticasone propionate and beclomethasone dipropionate. Arch Dis Child 1993; 68:673-6.
21.Merkus PJ, van Essen-Zandvliet EE, Duiverman EJ, van Houwelingen HC, Kerrebijn KF, Quanjer PH.
Long-term effect of inhaled corticosteroids on growth rate in adolescents with asthma. Pediatrics 1993; 91:1121-6.
22.Bloom CI, Yang F, Hubbard R, Majeed A, Wedzicha JA. Association of Dose of Inhaled Corticosteroids and Frequency of Adverse Events. Am J Respir Crit Care Med 2024 Aug 1. doi: 10.1164/rccm.202402-0368OC. Epub ahead of print. PMID: 39088770.
23.Ayodele OA, Cabral HJ, McManus DD, Jick SS. Glucocorticoids and Risk of Venous Thromboembolism in Asthma Patients Aged 20-59 Years in the United Kingdom's CPRD 1995-2015. Clin Epidemiol 2022; 14:83-93.
24.Wagner J, Langlois F, Lim DST, McCartney S, Fleseriu M. Hypercoagulability and Risk of Venous Thromboembolic Events in Endogenous Cushing's Syndrome: A Systematic Meta-Analysis. Front Endocrinol (Lausanne). 2019; 9:805.
25.Capewell S, Reynolds S, Shuttleworth D, Edwards C, Finlay AY. Purpura and dermal thinning associated with high-dose inhaled corticosteroids. Br Med J 1990; 300:1548-51.
26.Autio P, Karjalainen J, Risteli L, Kiistala U, Oikarinen A. Effects of an inhaled steroid (budesonide) on skin collagen synthesis of asthma patients in vivo. Am J Respir Crit Care Med 1996; 153:1172-5.
27.Haapasaari K, Rossi O, Risteli J, Oikarinen A. Effects of long-term inhaled corticosteroids on skin collagen synthesis and thickness in asthmatic patients. Eur Respir J 1998; 11:139-43.
28.Brusselle GG, Koppelman GH. Biologic Therapies for Severe Asthma. N Engl J Med 2022; 386:157-171.
|
|
Home
 Design by Walter Serralheiro Design by Walter Serralheiro
|
|
|